2020/5/1 レムデシビル、5月にも特例承認
安倍晋三首相は4月27日の衆参両院の本会議で、新型コロナウイルス治療薬の候補であるRemdesivirを「間もなく薬事承認が可能となる見込みだ」と説明した。
付記 Gilead
Sciencesが5月4日に承認を申請し、厚生労働省は5月7日、Remdesivirを「特例承認」した。
厚労相は、「いつ日本に届くのか確定した情報はない」とし、「必要な量の確保に向けて努力したい」と述べた。
薬事・食品衛生審議会は、有効性や安全性についての情報は極めて限られているとし、患者に文書で同意を得ることや、腎機能や肝機能の検査を毎日行うことなどを条件とした。最大10日間投与する。
主な投与経験をもとに、現時点では原則として重症患者を対象に投与を行うこととしている。集中治療室(ICU)に入っている患者、気管挿管されている患者、ECMOを導入している患者が対象となる。
下記のとおり、ウイルスの細胞内での遺伝子複製を阻害することで増殖を防ぐRNAポリメラーゼ阻害剤であり、本来は初期の患者に効くものである。
付記
「レムデシビル」(商品名ベクルリー)は2021年8月12日付で薬価収載されて保険適用になった
。10月にも一般流通を開始する。これまでは流通量が限られるとして厚生労働省が買い上げて医療機関に配分していた。
1瓶(100ミリグラム)の薬価は約6万3000円だが、新型コロナは指定感染症のため、保険適用後も患者負担は生じない。
日本が開発した抗インフルエンザ薬「アビガン」の承認も急ぐと強調した。「希望する患者への使用をできる限り拡大し、可能な限り早期の薬事承認をすべく努力している。すでに2000例以上投与され、症状改善に効果があったと報告を受けている」と指摘した。
現在、Remdesivirが承認された国・地域は無いが、ドイツや米国では5月中旬までに承認される見通しで、厚生労働省は海外で先に承認された場合、日本での審査を短縮する「特例承認」を適用する。
特例承認は、①国民の生命及び健康に重大な影響を与える恐れがある疾病が蔓延し、緊急に使用する必要がある
②日本と同等の審査水準がある外国で承認されている――
ことを条件に、通常は1年ほどかかる審査期間を短縮して承認できる制度。
日本人における有効性及び安全性の評価を行うため、原則として日本国内で実施された臨床試験データを併せて提出することを求めている。
下記の通り、Remdesivirについては日本の医療機関も治験に参加している。
付記 米食品医薬品局は5月1日、Remdesivirを症状の重い入院患者に投与する緊急使用を許可した。
日本で「特例承認」を適用する検討が加速する可能性があるが、日本向けの供給数量は限られているとされる。
アビガンは2014年3月24日に製造販売承認を取得したが、新型又は再興型インフルエンザウイルス感染症が発生し、既存の抗インフルエンザ薬が無効又は効果不十分である場合に備え、新しいメカニズムのアビガンを使用可能な状況にしておくことは意義があると判断され、世界に先駆けて国内で承認となったもので、厳しい条件がついている。
新型コロナウイルス用としては日本で未承認だが、世界のどの国でも承認を受けていない。このため、「海外で先に承認された場合、日本での審査を短縮する特例承認」が適用されず、所定の手続きによる承認が必要となる。
厚労省は、過去の薬害エイズ事件などの経験から、正規の手続きを短縮した承認には消極的であるとされる。
付記
新型コロナウイルス感染症の治療薬について、日本医師会の有識者会議(座長=永井良三・自治医科大学長)は18日、「科学を軽視した判断は最終的に国民の健康にとって害悪」だとして、適切な臨床試験を経て承認の手続きを進めるよう求める声明を公表した。国が早期承認を目指す新型インフルエンザ治療薬「アビガン」を念頭に、拙速に特例的な承認を行うべきではないと提言した。
声明は、科学的根拠の不十分な候補薬について「有事だから良い、ということには断じてならない」と指摘。自然に回復する患者も多いため、症例数の多い臨床試験が必要だとした。妊娠中の女性が服用して胎児に重い先天異常を引き起こしたかつてのサリドマイド薬害も引き合いに「数々の薬害事件を忘れてはならない」と強い懸念を示した。
有識者会議のメンバーで、国立国際医療研究センターの國土典宏理事長は「既存薬ならば、データがそろうまで適応外使用も可能だ。一度承認されれば有効性の検証は難しくなる」と警鐘を鳴らす。
新型コロナウイルス感染症の治療薬について、日本医師会の有識者会議(座長=永井良三・自治医科大学長)は18日、「科学を軽視した判断は最終的に国民の健康にとって害悪」だとして、適切な臨床試験を経て承認の手続きを進めるよう求める声明を公表した。国が早期承認を目指す新型インフルエンザ治療薬「アビガン」を念頭に、拙速に特例的な承認を行うべきではないと提言した。
声明は、科学的根拠の不十分な候補薬について「有事だから良い、ということには断じてならない」と指摘。自然に回復する患者も多いため、症例数の多い臨床試験が必要だとした。妊娠中の女性が服用して胎児に重い先天異常を引き起こしたかつてのサリドマイド薬害も引き合いに「数々の薬害事件を忘れてはならない」と強い懸念を示した。
有識者会議のメンバーで、国立国際医療研究センターの國土典宏理事長は「既存薬ならば、データがそろうまで適応外使用も可能だ。一度承認されれば有効性の検証は難しくなる」と警鐘を鳴らす。
日本医師会の有識者会議は5月18日、「科学を軽視した判断は最終的に国民の健康にとって害悪」だとして、適切な臨床試験を経て承認の手続きを進めるよう求める声明を公表した。
「アビガン」を念頭に、拙速に特例的な承認を行うべきではないと提言した。
科学的根拠の不十分な候補薬について「有事だから良い、ということには断じてならない」と指摘。自然に回復する患者も多いため、症例数の多い臨床試験が必要だとした。
妊娠中の女性が服用して胎児に重い先天異常を引き起こしたかつてのサリドマイド薬害も引き合いに「数々の薬害事件を忘れてはならない」と強い懸念を示した。
ーーー
RemdesivirはGilead
Sciencesがもともとエボラ出血熱を対象に開発を進めていた低分子化合物。
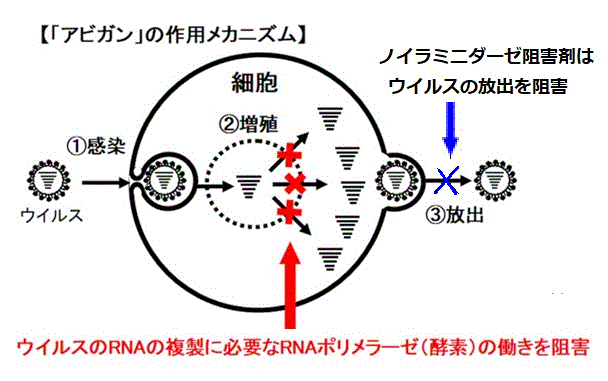
現在、治療に用いられている抗ウイルス剤はノイラミニダーゼ阻害剤(Neuraminidase
inhibitors)で、増殖されたウイルスの放出を阻害して感染の拡大を防ぐ。
これに対し、Remdesivirはアビガン
と同じく、ウイルスの細胞内での遺伝子複製を阻害することで増殖を防ぐRNAポリメラーゼ阻害剤である。
Remdesivirは体内で代謝を受けてその活性型GS-441524に変わる。GS-441524は、ウイルスのRNAポリメラーゼ
を混乱させて、ウイルスRNA産生の減少を引き起こす。
このことから、両剤とも早期の患者に有効である。
付記 Remdesivirは静脈内投与する点滴注射薬
(重症者向け)
アビガンは錠剤 (軽症者向け)
米国立衛生研究所(NIH)は2月25日にGilead
Sciencesが開発した抗ウイルス薬Remdesivirの世界規模での治験計画を発表した。世界50カ所で偽薬とremdesivir
を患者に投与し、治療効果を検証するもので、国立国際医療研究センター(NCGM)はこれに参加している。
WHOを中心とした研究開発チームが抗エイズウイルス(HIV)薬のLopinavirとRitonavir の合剤と、Remdesivir を試験している。
中国を視察しているWHOのBruce Aylward
事務局長補は2月24日、「現時点で有効と思われる唯一の薬がある。それは
remdesivirだ」と述べた。
Gilead SciencesではRemdesivir
の効果についてさらに多くのデータを集めるため、これまでの治験とは別に、新たに横浜市立市民病院など国内の3つの医療機関と連携し、新型コロナウイルスの患者に薬の投与を行う治験を4月14日から始めた
。治験は、日本だけでなく、アメリカやイタリアなどの合わせて4000人を対象に、重症や中程度などのグループに分けて薬の安全性や有効性を確かめる。
ヘルスケア・ライフサイエンス系専門メディアのSTATは4月16日、COVID-19の中等度と重度の患者を対象に実施しているRemdesivirの臨床試験の結果を報じた。
University of Chicago Medicine
は125名の患者(うち113名が重症)でテストをした。このうち、ほとんどが既に退院した。死亡は2名だけであったという。
対照群にプラセボ群は置いていない。
2020/4/17 Remdesivirの臨床試験で好結果
Gilead
Sciencesは4月29日、「有望なデータが得られつつある」と発表した。承認申請前の最終段階の第3相臨床試験を2つ実施しているが、そのうちの一つ。
397人の患者を対象に臨床試験を行い、投与初日から14日目の状況を調べた。
5日間投与したグループでは60%の患者が退院し、10日間の投与では52%が退院した。治療期間が短くてすむ可能性が示されたとする。
また、症状が出てから10日以内に投与されたグループの方が、それより後に投与されたグループに比べ、症状が改善したケースが多かった。
米国立衛生研究所(NIH)傘下の国立アレルギー・感染症研究所は4月29日、Remdesivirの臨床試験で、患者の回復スピードが31%早まったとの暫定結果が得られたと明らかにした。
新型コロナ感染症の入院患者1063人を対象に実施した臨床試験では、Remdesivirを投与した患者が11日で回復したのに対し、プラセボ(偽薬)を投与した場合は15日を要した。
死亡した人の割合を比較しても低く抑えられた。
なお、中国のチームが4月29日に、「明確な治療効果が確認できなかった」とする臨床試験の結果を英医学誌ランセットに発表した。
但し、中国の感染者が減って予定した参加人数に達せず、試験を途中で打ち切ったため有効性を評価するにはさらにデータが必要としている。投与が早いと症状の改善が望める可能性は示された。
2020/5/2 欧州で新型コロナ感染の子供に「川崎病」に似た症例
WHOは4月29日、新型コロナウイルスに感染した子どもの中で、血管に炎症が起きて発疹や目の充血などを起こす「川崎病」に似た症例が複数報告され、各国と連携しながら注視していく考えを示した。
ヨーロッパ各国では全身の血管に炎症が起こる「川崎病」に似た症状のある子どもがこのところ相次いで確認されている。
英国のハンコック保健相は4月28日、同国で既往症のない子どもが珍しい炎症性症候群で死亡するケースが複数でており、研究者らがCOVID-19と関連があるとみていると述べた。子どもは病院に搬送されてきた時に高熱と動脈部の腫れの症状があった。
ハンコック保健相は、「死亡した何人かの子どもには既往症がなかった。COVID-19ウイルスが原因かもしれないが、検査で陽性反応がでなかった人もいる」とし、「引き続き調査を進める」と述べた。
同様の報告はスペインやベルギーなど各国で挙がっていて、フランスでは、今月半ばからこれまでに15ほどの症例の報告があった。
イタリアの専門家は、「今の段階でははっきりしていないが、どちらにせよCovid19が川崎病と同じ症状を引き起こすことはあり得る。ウィルスに感染したのをきっかけにそれを防ごうとする免疫反応として川崎病の症状が出るのかもしれない」としている。
ーーー
「川崎病」は、1967年
に小児科医の川崎富作医師が発表した、手足の指先から皮膚がむける症状を伴う小児の「急性熱性皮膚粘膜りんぱ腺症候群」が新しい病気であることがわかり、博士の名前をとって川崎病という病名にな
った。
川崎病は急性熱性疾患(急性期)と冠動脈障害を主とした心疾患(後遺症)の2つの疾患をもつ。
急性期の症状は、下記の通り。
- 5日以上続く発熱(38度以上)
- 発疹
- 両方の目が赤くなる(両側眼球結膜充血)
- 唇が赤くなったり、苺舌がみられる
- 病気の初期に手足がはれたり、手のひらや足底が赤くなったりする
熱が下がってから、手足の指先から皮膚がむける膜様落屑(まくようらくせつ)がある
- 片側の首のリンパ節がはれる
重症の血管炎から後遺症として冠動脈障害や心筋梗塞を引き起こす。
冠状動脈(冠動脈)の血管壁の構造がこの反応によって破壊されてもろくなり、もろくなった部分が拡大して瘤となることがある。(冠動脈障害)
冠動脈障害が原因になって、この動脈が詰まり、心筋梗塞がおこる場合がある。
(通常、心筋梗塞は動脈硬化からくる成人病だが、こどもでも川崎病による冠動脈障害が原因となっておこる場合がある。)
この病気は世界各地で報告されていて、とくに日本人、日系アメリカ人、韓国人などアジア系の人々に多くみられる。
原因はまだ不明だが、ウイルスや細菌に感染したのをきっかけにそれを防ごうとする免疫反応がおこり、全身の中小の血管に炎症が生じるのではないかと考えられてい
る。
細菌などが侵入すると、それが刺激になって白血球が増え、血管の壁(血管壁)に集まる。
この状態が血管炎で、炎症が強すぎると白血球から出る酵素によって血管壁は傷んでしまう。
2020/5/4 COVID-19とBCG接種(その4)
さきに2019/4/7「BCGはCOVID-19に効くか?」、2020/4/13
BCGとCOVID-19(補足)、2020/4/27
BCGとCOVID-19(その3)を書いた。BCGとCOVID-19の関連についての仮説を確かめた。
そのまとめ:
1) BCG全員注射をやったことのない4か国の死者は極めて多い。
2) 現在もBCG注射をしている国は、現在はしていない国境を接する隣国に比し、著しくひくい。
3) BCG全員注射をやったことのない4か国(160人以上)と、現在もやっている残りの国(5人未満)との差は驚くほど大きい。
4)ワクチンのうち、ソ連株、日本株を使う国は死亡率が低い。死亡率が高い国はDenmark株が多い。
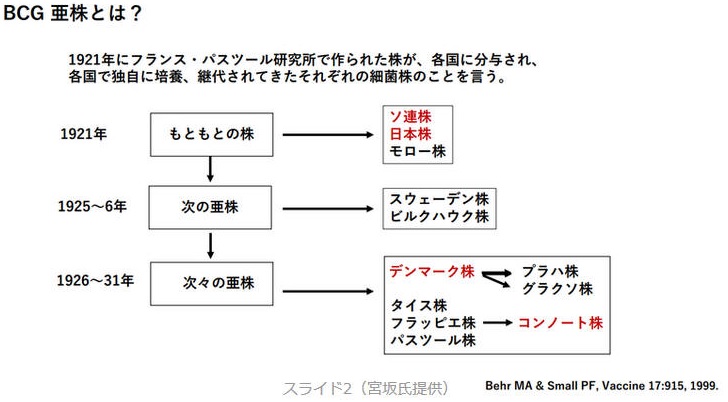
日本株とソ連株は、デンマーク株と細胞膜構成成分が異なる。
日本株とソ連株は他の亜株に比し、結核に対して免疫を起こす力は同程度だが、生菌数が非常に多い。
ーーー
ここで問題に気が付いた。「現在もやっている国」と「現在はしていない国」の対比は正しくない。
いつ始めたか、いつ止めたかにより、国民のどれだけが接種をしているかに差がある。
東京工大のチームがmedRxivに発表した論文
Relationship between COVID-19 death toll doubling time and national BCG
vaccination policyを見つけた。
BCG接種国と非接種国で死亡率が大きく異なるが、接種国の中では東京株と他の株でも大きな差があるとする。
死亡数が倍になる日数が東京株の8カ国平均で7.2日であるのに対し、他の株の34か国平均は5.5日である。
この論文には、国別に集団接種を実施した期間、集団接種を受けた人の現在の年齢(何歳から何歳まで)とその国のBCG株の種類が記載されている。
これにより、全人口のうちのどれ位が接種をうけているかが分かる。
前の記事で、隣接する英国(現在はしていない)とアイルランド(最近まで実施)との差が急速に近づいているとした。
実際には英国では延べ53年間接種を実施(最初の年に12、3歳児までを実施)、アイルランドとの差は少ない。
(今回の表ではアイルランドは1950s-2003?となっているが、前回資料では1937-2015となっている)
スウェーデン(延べ36年)と隣接するノルウェー(延べ63年)では死亡率に差がある。
札幌医科大学医学部の人口あたりの新型コロナウイルス死者数の推移から最新(4月30日)の人口100万人当たり死者数を使用し、世界58カ国を死者の多い順に並べた。(ベトナムを追加)
1) 集団接種をしたことのない5カ国(ベルギー、イタリー、オランダ、米国、カナダ)の死亡率は極めて高い。
カナダは比較的少ないが、任意の接種で2012年から日本株を使っている。
2) 東京株接種の国の死亡率は極めて低い。
イラクは隣接するイランに比し、極めて低い。
3) ロシア(ソ連)株は日本株に近く、死亡率は低いが、東京株よりは高い。
4) 欧州はデンマーク株(Danish 1331)が多いが、接種の延べ年数が高くても(人口の多くが接種を受けている)死亡率が極めて高い。
それでも、過去にやっていないスペインと比べ、隣接するポルトガルの死亡率は低い。
人口100万人当たり死者数 順位 (2020/4/30時点)
参考 5/19、6/5 時点の死者数
| 国 |
人口千人 |
集団接種
実施期間 |
接種者
現年齢 |
接種
延年数 |
BCG株 |
100万人
当たり死者 |
|
ベルギー |
11,590 |
ー |
ー |
ー |
Pasteur 1173 |
647 |
| スペイン |
46,775 |
1965-1981 |
39-55 |
17 |
Danish 1331 |
519 |
|
イタリー |
60,462 |
ー |
ー |
ー |
Danish 1331 |
458 |
|
英国 |
67,886 |
1953-2005 |
28-80 |
53 |
Glaxo |
384 |
| フランス |
65,274 |
1950-2007 |
13-70 |
58 |
Danish 1331 |
369 |
|
オランダ |
17135 |
ー |
ー |
ー |
Bulgaria |
275 |
| スウエーデン |
10,099 |
1940-1975 |
45-80 |
36 |
Danish 1331 |
244 |
| アイルランド |
4,938 |
1950s-2003? |
17-60+ |
44 |
Danish 1331 |
241 |
|
米国 |
331,003 |
ー |
ー |
ー |
|
184 |
| スイス |
8,655 |
1960s-1987 |
33-50+ |
18 |
Merieux
(Danish) |
163 |
| ポルトガル |
10,197 |
1965-2015 |
5-55 |
51 |
Danish 1331 |
95 |
|
カナダ |
37,742 |
ー |
ー |
ー |
Connaught(-2012),
Tokyo 172-1(2012--) |
79 |
| デンマーク |
5,792 |
1946-1986 |
34-74 |
41 |
Danish 1331 |
76 |
| ドイツ |
83,784 |
1961-1998 |
22-59 |
38 |
Danish 1331
旧東独はRussia |
75 |
| イラン |
83,993 |
<1990-2018+ |
0-30+ |
31 |
Pasteur
1173 P2 |
71 |
| オーストリア |
9,006 |
1952-1990 |
30-68 |
39 |
|
64 |
| エクアドル |
17,643 |
<1995-2018+ |
0-25+ |
26 |
Russia-Bulgaria |
50 |
| トルコ |
84,339 |
1952-2018+ |
0-68 |
69 |
Serum Inst. India (Russia) |
45 |
| スロベニア |
2,079 |
1947-2005 |
15-73 |
59 |
Danish 1331 |
43 |
| パナマ |
4,315 |
<1980-2018+ |
0-40+ |
41 |
Russia-Bulgaria |
41 |
| ノルウェー |
5,421 |
1947-2009 |
11-73 |
63 |
Danish 1331 |
37 |
| フィンランド |
5,541 |
1941-2006 |
14-79 |
66 |
Glaxo,
Danish 1331 |
37 |
| ルーマニア |
19,238 |
1928-2018+ |
0-92 |
93 |
Romania BCG
substrain |
35 |
| マケドニア |
2,083 |
<1993-2018+ |
0-27+ |
28 |
Toronto
Canada (Connaught) |
35 |
| ハンガリー |
9,660 |
1953-2018+ |
0-67 |
68 |
Danish 1331 |
32 |
| プエルトリコ |
2,861 |
|
|
|
|
30 |
| ペルー |
32,972 |
<1990-2018+ |
0-30+ |
31 |
Danish 1331 |
29 |
| モルドバ |
4,034 |
<1992-2018+ |
0-28+ |
29 |
|
28 |
| ドミニカ |
10,848 |
<1995-2018+ |
0-30+ |
31 |
Russia-Bulgaria |
27 |
| ブラジル |
212,559 |
<1990-2018+ |
0-30+ |
31 |
Moreau |
26 |
| イスラエル |
8,655 |
1955-1982 |
38-65 |
28 |
|
25 |
| チェコ |
10,709 |
1953-2010 |
10-67 |
58 |
Moreau |
21 |
| セルビア |
8,737 |
<1992-2018+ |
0-28+ |
29 |
Pasteur
1173 P2 |
19 |
| ポーランド |
37,847 |
1955-2018+ |
0-65 |
66 |
Danish 1331 |
16 |
| メキシコ |
128,933 |
1951-2018+ |
0-69 |
70 |
Danish 1331 |
13 |
| ギリシャ |
10,423 |
<1980-2014+ |
12-46+ |
35 |
Danish 1331 |
13 |
| チリ |
19,116 |
<1980-2018+ |
0-40+ |
41 |
Danish 1331 |
11 |
| アルジェリア |
43,851 |
<1985-2018+ |
0-35+ |
36 |
|
10. |
| ロシア |
145,934 |
<1992-2018+ |
0-28+ |
29 |
Russia |
7 |
| ウクライナ |
43,734 |
<1992-2018+ |
0-28+ |
29 |
Bulgaria
NCIPD |
6 |
| コロンビア |
50,883 |
<1980-2018+ |
0-40+ |
41 |
Pasteur
1173 |
5 |
|
フィリッピン |
109,851 |
1979-2018+ |
0-41 |
42 |
Tokyo 172-1
and others |
5 |
|
韓国 |
51,269 |
1970s-1985? |
0-40+ |
41 |
Tokyo 172-1 |
5 |
| アルゼンチン |
45,196 |
<1985-2018+ |
0-35+ |
36 |
Anlis
Malbran (Pasteur) |
5 |
| モロッコ |
36,911 |
1949-2018+ |
0-71 |
72 |
|
5 |
|
サウジ |
34,814 |
<1985-2018+ |
0-35+ |
36 |
Pasteur, Danish 1331,
Tokyo 172-1 |
5 |
| エジプト |
102,334 |
<1990-2018+ |
0-30+ |
31 |
|
4 |
| 豪州 |
25,500 |
1950s-1985? |
40-70 |
31 |
Connaught
(until 2010s) |
4 |
|
日本 |
126,476 |
<1951-2020 |
0-69+ |
70 |
Tokyo 172-1 |
3 |
| 中国 |
1,439,324 |
1949-2018+ |
0-71 |
72 |
Shanghai
D2PB302 |
3 |
|
マレーシア |
32,366 |
<1980-2018+ |
0-40+ |
41 |
Tokyo 172-1 |
3 |
| インドネシア |
273,524 |
<1990-2018+ |
0-30+ |
31 |
Pasteur
1173 |
3 |
|
イラク |
40,223 |
<1980-2018+ |
0-40+ |
41 |
Tokyo 172-1 |
2 |
| 南アフリカ |
59,309 |
<1995-2011+ |
0-25+ |
26 |
Danish 1331 |
2 |
|
パキスタン |
220,892 |
1978-2018+ |
0-40 |
41 |
Danish 1331(-2007)
Tokyo172-1(2008-) |
2 |
|
バングラデシュ |
164,689 |
<1990-2018+ |
0-30+ |
31 |
Serum Inst. India (Russia)
Tokyo 172-1 |
1 |
| インド |
1,380,004 |
1951-2018+ |
0-69 |
70 |
Danish 1331 |
1 |
| ベトナム |
94,670 |
30年以上前から |
|
|
0 |
ベトナム(いまだに死者ゼロ)の場合は、完全な封じ込めが成功した例である。
2020/4/28 COVID-19対策、ベトナムの場合
上記のデータから見ると、COVID-19による死者数とBCG接種の関係は偶然の一致とはとても思えない。
現在、世界各地でこの研究が行われている。
なお、上表では日本の集団接種は<1951年となっているが、実際は全員接種である。
1949年にBCGワクチンによる結核予防接種が法制化されたが、30歳未満の人に毎年ツベルクリン反応検査を行い、免疫が確認されなかった場合は繰り返し接種を行っている。
2013年に接種対象者が生後1歳に達するまでに変更された。
2020/5/5 50 ℃で水素と窒素からアンモニアを合成する新触媒
東京工業大学 科学技術創成研究院の原亨和教授、元素戦略研究センター長の細野秀雄栄誉教授らは4月27日、50
℃未満の温度で水素と窒素からアンモニアを合成する新触媒の開発に成功したと発表した。
豊富なカルシウムに水素とフッ素が結合した物質「水素化フッ素化カルシウム(CaFH)」とルテニウム(Ru)ナノ粒子の複合材料「Ru/CaFH」で、室温で水素と窒素からアンモニアを合成できる。
現在、アンモニアはHaber–Bosch
法により、窒素ガスと水素ガスから工業的に合成されているが、高温・高圧の過酷な反応条件(使用されている鉄系触媒では約400~500°Cかつ14~30MPa)に加え、原料となる水素ガスが化石燃料由来であり、大量のCO2を発生させ、水素ガスの製造には多大なエネルギーを消費する。
新触媒により、自然エネルギーを使った温室効果ガスのCO2排出ゼロにつながることが期待される。
本研究成果はNature communicationsオンライン速報版に4月24日に掲載された。
Solid solution for catalytic ammonia synthesis from nitrogen and hydrogen
gases at 50 °C
ーーー
なお、既報の通り、東大大学院工学系研究科が2019年4月25日、常温・常圧の温和な反応条件下で窒素ガスと水からアンモニアを合成する世界初の反応の開発に成功したと発表している。
モリブデン触媒を用い、窒素ガスおよびプロトン(H+)源として水、還元剤としてヨウ化サマリウムを用いることで、常温・常圧の反応条件下で世界最高の触媒活性を達成した。
2019/5/3 世界で初めて窒素ガスと水からのアンモニア合成に成功
ーーー
アンモニア合成の難関は、窒素分子(N2) を窒素原子(N) にまで分解することである。
窒素分子(N2)は2つの窒素原子が三重結合という強い結合で結ばれているため、非常に安定な分子で、反応性が乏しく、ほとんどの生物は大気中の窒素を直接利用することができない。
マメ科の植物に共生する細菌が持つ酵素「ニトロゲナーゼ」のみが常温・常圧で窒素の三重結合を断ち切って窒素をアンモニアへと変換している。
窒素分子の分解には、鉄などの遷移金属からN2へ電子を一時的に与えることが必要であるが、そのためには金属に電子を与える電子供与材料が必要となる。
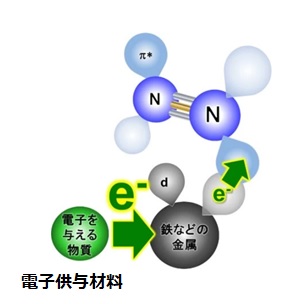
従来のアンモニア合成の鉄触媒では酸化カリウム(K2O)が電子供与材料として使われる。しかし、100~200 ℃で電子を与える力が弱まり、作動しなくなる。
ーーー
チームはありふれた脱水材の水素化カルシウムCaH2に着目した。これ自体は低温では役に立たない。
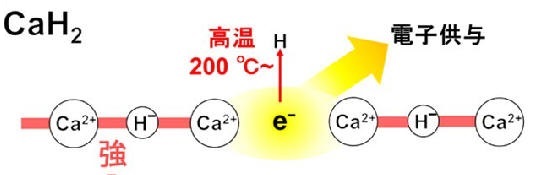
CaH2はCa2+の陽イオンと水素の陰イオンH–(ヒドリドイオン)が結合したイオン性固体である。
200 ℃より高い温度にすると一部のH–が水素分子として抜け、電子をCa2+イオンの周りに残す。
この状態の電子はアルカリ金属並みの電子供与能をもつため、この電子で遷移金属の電子供与をブーストすればN2分子は窒素原子まで分解できる。
しかし、Ca2+—H–のイオン結合エネルギーが強いため、低温で使うことができない。
対策として、Ca2+とより強い結合をつくる陰イオンを入れ、Ca2+—H–の結合エネルギーを弱める。
Ca2+—F–の結合エネルギーはCa2+—H–のそれの2倍の強度をもつ
。
CaH2のヒドリドイオンの一部をF–で置き換え、水素化フッ素化カルシウムCaFHをつくった。
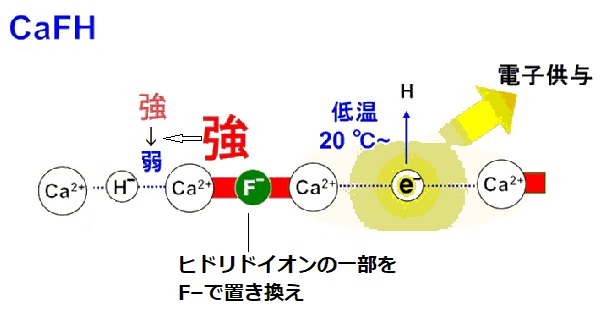
この場合、Ca2+—H–のイオン結合エネルギーが弱まり、水素の陰イオンH–(ヒドリドイオン)は低温で水素分子として脱離し、低温で強い電子供与能を発揮する。
実際に合成したCaFHでは室温程度からヒドリドイオンが水素分子として抜けることが確認された。
チームは、この水素化フッ素化カルシウム(CaFH)とルテニウム(Ru)ナノ粒子の複合材料「Ru/CaFH」で触媒を作った。
実験結果は下記の通り。
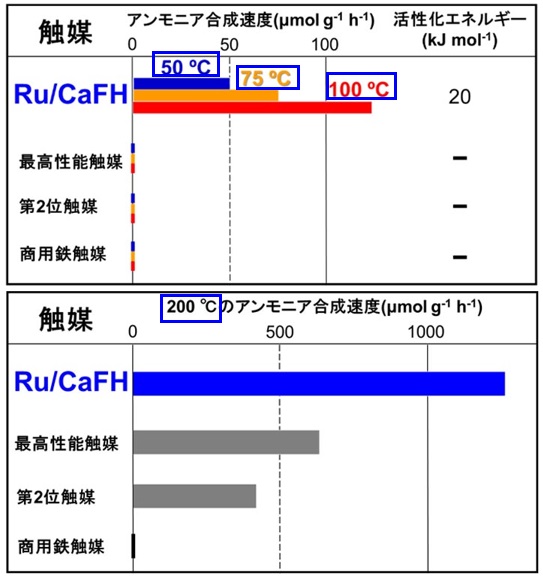
この触媒は100 ℃以下でもアンモニアを合成し、50
℃でさえ作動していることがわかった。
現在のアンモニア生産に使われている商用の鉄触媒、そして、つい最近発表された最高性能の触媒(Ru/BaO-BaH2)、第2位の触媒(Ru/CaH2)
は100 ℃以下の温度では全く作動しない。
他の触媒が機能する200
℃での場合でも、この触媒は最高性能触媒の2倍を越えており、高い温度でも既存触媒を凌駕している。
なお、Ru/CaFHの活性化エネルギー(反応を進めるために必要なエネルギー)は20 kJ
mol-1であり、これまで報告され現在のアンモニア生産にてできたアンモニア合成触媒の1/2程度にしか過ぎない。
また、Ru/CaFHは安定な触媒であり、300 ℃を越える反応温度でも900時間以上アンモニア合成速度の低下なく、作動し続ける。
原教授のコメント
今回の研究に対する私たちの感想は、「社会が求めるアンモニア生産のきっかけを見つけた」に過ぎません。
しかし、化石資源を使わずに肥料を生産し、人々に食糧を届けることが単なる夢想ではなくなり、現実味を帯びてきました。
従来の触媒開発がしてきた性能向上をたどることによって、私達のアプローチ・触媒は真に地球・社会・人が求めるアンモニア生産に繋がると考えています。
2020/5/6 COVID-19の致死的急性呼吸器不全症候群の原因はサイトカインストーム
国立研究開発法人量子科学技術研究開発機構の平野俊夫理事長は4月15日、北海道大学遺伝子病制御研究所の村上正晃教授と共同で、新型コロナウイルスに関する論文を発表した。
COVID-19で肺炎を起こしても軽い症状で治る場合もあるが、重篤化する人もいる。特に重症化したCOVID-19に発症する急性呼吸器不全は致死率が高い。
この原因は免疫系の過剰な生体防御反応のサイトカインストームが原因であることを見付けた。
論文はImmunity に掲載された。COVID-19: A New Virus, but a Familiar Receptor and Cytokine
Release Syndrome
論文のポイント:
- COVID-19に伴う致死的な急性呼吸器不全症候群(ARDS: Acute
Respiratory Distress Syndrome)は、免疫系の過剰な生体防御反応であるサイトカインストームが原因であると考えられる。
- サイトカインストームは、遺伝子の転写因子であるNF-kBとSTAT3の協調作用により、免疫関連タンパク質であるインターロイキン6(IL-6)の増幅回路(IL-6アンプ)が活性化され、炎症性サイトカインの産生が異常に増加し起こる。
- COVID-19にみられる急性呼吸器不全症候群の治療薬の標的としてIL-6
アンプが有望であり、IL-6-STAT3経路の阻害が有効である。
すでに遺伝子導入T細胞(CAR-T)療法におけるサイトカイン放出症候群の治療に使用されており、かつIL-6アンプを阻害できる抗IL-6受容体抗体
も有望である。
最近のNature と Cell の論文で下記の点が明らかになっている。
1)SARS-CoV-2ウイルスの表面に存在するスパイクタンパクは、細胞表面のACE2を受容体として結合するが、細胞内に入って感染するためにはスパイクタンパクが細胞表面のタンパク分解酵素であるTMPRSS2により切断
・分割 (開裂活性化) される必要がある。
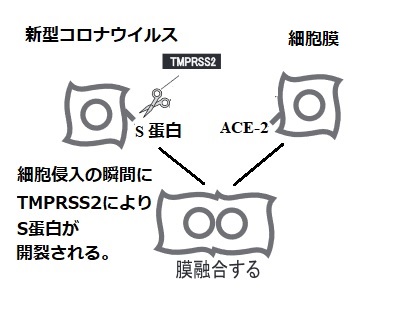
2)その後切断・分割され活性化したスパイクタンパクがウイルス膜と細胞膜の融合を引き起こす結果、ウイルスはACE2とともに細胞内に取り込まれる。
3)TMPRSS2の阻害剤はウイルス感染モデル実験系においてウイルスの細胞内取り込みを阻止した。またACE2に対する抗体もウイルスの細胞内取り込みを阻止した。
したがって、SARS-CoV-2ウイルスとACE2との結合を抑制する分子や、TMPRSS2の阻害剤はウイルス感染を抑制する効果が期待され、ウイルス感染の初期には有効な治療薬になる可能性がある。
また、スパイクタンパクに対する抗体、スパイクタンパク以外のウイルス膜タンパクに対する抗体やサーズウイルスや新型コロナウイルスから治癒した患者に存在する抗体なども期待される。
一方、感染後期に生じる致死的な急性呼吸器不全ARDSは、ウイルスが減少し始めた頃に生じる
。
筆者らは、これを、ウイルスそのものによるものではないと考え、過剰な生体反応であるサイトカインストームにより引き起こされるサイトカインリリース症候群CRSである
とする。
気管支・気道上皮細胞にてACE2に結合したSARS-CoV-2ウイルスは、TMPRSS2の作用により細胞内に取り込まれる。
転写因子であるNF-kBとSTAT3の協調作用により、インターロイキン6(IL-6)の増幅回路(IL-6アンプ)が活性化され、炎症性サイトカインの産生が異常に増加するサイトカインストームが発生することによりが発症するという仕組みを提唱した。
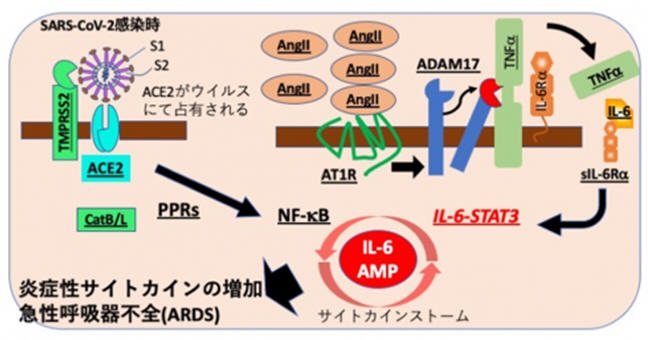
NF-kB
は炎症反応で中心的な役割を果たす転写因子で、病気を引き起こすような過剰な活性化は、NF-kB活性化と同時にIL-6-STAT3経路の活性化が必要である。
STAT3 (Signal Transducer and Activator of Transcription
3) は転写因子であり核内で機能する。炎症時のSTAT3活性化因子はIL-6で、核内でNF-kBと会合してNF-kBの活性を増強する。
SARS-CoV-2ウイルスが細胞内に取り込まれると、ウイルス分子の構造を認識した細胞のパターン認識受容体(PPRs)が活性化し、下流のNF-kB経路が活性化する。
さらに、感染に伴って本来ACE2に結合して分解されるアンジオテンシン(AngII)が血中に増加し、アンジオテンシン受容体1(AT1R)からの信号が過剰となる。
活性化されたAT1R信号は、蛋白質分解酵素であるADAM17を活性化し、細胞膜型のTNFa、IL-6Ra、増殖因子などの炎症関連分子を可溶性のものに変換する。
可溶性の炎症関連分子(図ではsIL-6Ra)は、気管支・肺胞上皮細胞、血管内皮細胞を含む非免疫系細胞にてNF-kBとIL-6-STAT3を同時に活性化し、IL-6アンプを活性化、これらの細胞の局所にて過剰なサイトカインが産生される。
その結果、サイトカインリリース症候群CRSが引き起こされ、COVID-19にみられる致死的な急性呼吸器不全症候群ARDSが発症すると考えられる
。
感染初期は免疫力を高める必要があるが、重篤化すると逆に免疫を抑える治療が必要になる。
感染後期に見られる致死的な急性呼吸器不全症候群の治療には、すでに遺伝子導入T細胞(CAR-T)療法におけるサイトカイン放出症候群の治療に使用されており、かつIL-6アンプを阻害できる抗IL-6受容体抗体
も有望である。
有望視されるのが、中外製薬のIL6 阻害薬「アクテムラ」(ヒト化抗ヒトIL-6レセプターモノクローナル抗体)で、関節リウマチ,
若年性特発性関節炎, 成人スチル病, 高安動脈炎・巨細胞性動脈炎, キャッスルマン病の治療に使われている。
中外製薬の親会社のRocheは3月19日、米国食品医薬品局(FDA)と連携し、重症COVID-19肺炎による入院患者を対象にActemra/RoActemraの第III相臨床試験を開始すると発表した。
Actemra/RoActemraについては、3月3日に中国国家衛生健康委員会(NHC)が発行したCOVID-19診断・治療計画第7版で言及されているが、安全性、有効性を確認する。
中外製薬は4月8日、「アクテムラ®点滴静注用80 mg、同200
mg、同400 mg」[一般名:トシリズマブ(遺伝子組換え)]について、COVID-19肺炎を対象とした国内第III相臨床試験を実施すると発表した。
付記
エーザイは7月1日、同社のTLR4(Toll-Like Receptor
4)拮抗剤エリトランが新型コロナウイルスのサイトカインストームを抑制の候補として臨床試験に入ると発表した。
カリフォルニア州のGlobal Coalition for Adaptive
Researchとエーザイが、University of Pittsburgh Medical
Centerと共同で臨床試験に入る。今後、日本を含む各国に拡大する。
エリトランは、細菌の感染に対する過剰炎症反応である重症敗血症の治療剤で、エーザイが創製したエンドトキシン拮抗剤。
細菌から放出されたエンドトキシンがその受容体であるTLR4に結合することを阻害することにより、TLR4が活性化すると引き起こされる受容体シグナルの伝達を防ぐ。その結果、炎症性サイトカインの遊離が阻害され、敗血症症状の発現が抑制される。
エリトランの安全性プロファイルは、重症セプシスを対象として実施した大規模な臨床第Ⅲ相試験で確認されている。
|
2020/5/7 米FDA、ロシュの新型コロナ抗体検査薬の緊急使用許可
スイス製薬大手Rocheは5月3日、新型コロナウイルスの抗体検査薬 Elecsys®
Anti-SARS-CoV-2
について米食品医薬品局(FDA)から緊急使用許可(Emergency Use Authorization :EUA)
を取得したと発表した。今月中にも欧米で数千万回分を提供する。日本でも5月中に承認申請する。
ドイツ政府は5月に300万個、それ以降は月500万個購入する契約を締結した。
新型コロナウイルス(SARS-CoV-2)に暴露した人々に存在する抗体を検出する。
ウイルスに感染した人、感染した可能性があるものの症状の発生を伴わなかった人を判別するのに役立つ。
また、免疫獲得の状態を判断することによって、業務従事の可否を判断する一助になり、経済活動の正常化に向けた道筋を描きやすくなる。
なお、WHOは4月24日のScientific
Brief で、抗体の存在を“immunity passport” や “risk-free certificate”
とする向きがあるが、今のところ抗体を得た人が再度罹らないとの科学的根拠はないと注意を促している。
韓国の中央防疫対策本部は4月12日、新型コロナウイルスによる感染症が完治し、隔離が解除された後、再び陽性判定を受けた人が計111人になったと発表した。
罹患して直っても(多分、抗体が出来ている筈)、再度罹患した。
2020/4/14
韓国でCOVID-19 回復後に再陽性111人
Elecsys
Anti-SARS-CoV-2は、血清および血漿中のSARS-CoV-2に対する抗体(IgGを含む)を検出し、免疫反応状態を判断する。
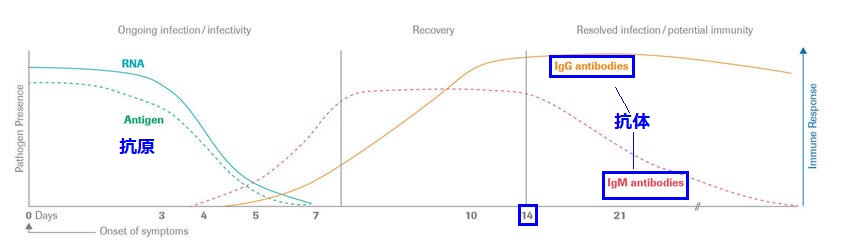
世界中の病院検査室ならびに検査会社において広く使用されているRocheの電気化学発光法免疫分析装置
コーバス(cobas
e 411 analyzer, cobas e 601 / cobas e 602 modules, cobas e 801 module)
によって検査することができる。
測定時間は約18分で、1時間当たり最大300テストの測定が実施できる。
同社は約5200人について臨床試験を実施した。PCR検査で新型コロナの感染が確認された人について14日後に検査したところ、正しく陽性と判断する感度(sensitivity)が100%で、正しく陰性と判断する特異度(specificity)は99.8%超と信頼性が極めて高い。
注射で採取した血液で検査を行うため、指先からの採血による検査よりも正確性が高いという。
簡易検査キットの場合、一般的な風邪の原因となるウイルスとコロナウイルスに対する抗体とを間違う可能性もあるが、Rocheのキットは新型コロナだけを高い精度で特定できるとされる。
Rocheは月間生産量を現在の5000万個から年末までに1億個以上に引き上げる。 |
2020/5/7 ファイザー、新型コロナウイルスワクチンの臨床試験を米国で開始
米製薬大手Pfizer Inc.は5月5日、ドイツのバイオ医薬スタートアップ企業のBioNTech
SE と共同開発する新型コロナウイルスの予防ワクチンの臨床試験(Phase1/2) を米国でも始めたと発表した。
4種類のRNA(リボ核酸)ワクチン候補 BNT162
をヒトに接種し、安全性を確認する。ドイツで先行して4月に同段階の治験を開始した。早ければ年内に数百万本を生産する。
ワクチンの臨床試験では通常、安全性の検証(Phase
1)から開始するが、今回はワクチン開発を加速化させるため安全性と免疫システムの反応(Phase 2) を同時に検証する。
先ず、NYU Grossman School of Medicine と
University of Maryland School of Medicineで始め、その後、University of Rochester Medical
Center/Rochester Regional Health とCincinnati Children’s Hospital Medical Center
で実施する。
健康な360人を18-55歳と65-85歳の2グループに分けて実施する。先ず、若いグループで安全性と免疫システムの反応が確認された時点で、高齢者層のグループの臨床試験を開始する。
世界各地でワクチンの開発が進められており、いくつかの種類があるが、同社のは「mRNAをベースにしたワクチン」で、抗原となるたんぱく質をmRNAで発現させ、それに対応した抗体が体内で産出されるよう促すもの。
|
 |
→ |
 |
それぞれ異なるmRNA構造と標的抗原を有する4種のワクチンをテストする。
4つのワクチン候補のうち2つは修飾ヌクレオシドmRNA (modRNA)を含み、1つはウリジン含有mRNA(uRNA)を含んでおり、4つめは自己増幅
mRNA(saRNA)を利用している。
まず、18~55歳の健常成人を約200名組み入れ、1~100
µgの用量を投与して今後の臨床試験の至適用量を検討するとともに、ワクチン候補の安全性と免疫原性を評価する。
加えて4つのワクチン候補のうち、uRNAまたはmodRNAを含む3つを反復投与した際の効果も評価する。
COVID-19感染症が重症化するリスクの高い被験者(65-85歳)は、本試験の2つ目のパートに組み入れる。
臨床試験に当たり、BioNTechがワクチンを提供する。
ーーー
BioNTech はオーストリアのPolymun
Scientificと組んで、ドイツのMainz及びIdar-Oberstein工場でmRNA を生産している。
Pfizer とBioNTech は2018年にインフルエンザ予防を目的としたmRNAワクチンの開発のために共同開発契約を結んだ。
この契約に基づき、両社は3月19日にコロナウイルスに対するmRNAワクチンの共同開発および流通(中国を除く)に関する覚書について合意した。
BioNTechのmRNAワクチンBNT162の開発を加速することを目的とする。米国とドイツを含む両社の複数の研究開発施設を活用する。
これを基に、今回の契約となった。
BioNTech は3月16日、Shanghai Fosun Pharmaceutical
(上海復星醫藥)との間で、BioNTechのCOVID-19のmRNAワクチン候補であるBNT162の中国での開発のための戦略的開発及び商業化協力契約を締結した。
BioNTechの供給するBNT162を使い、復星醫藥の中国における広範な開発、規制対応、商業化の能力を活用し、中国で共同で臨床試験を実施する。
中国で承認を得られた場合、復星醫藥が中国で販売する。中国以外の全世界での開発・販売権はBioNTech
が持つ。
なお、復星醫藥はBioNTech
に50百万ドルを出資した。
ーーー
臨床試験の成功を予想し、両社は供給体制を増強している。
Pfizerは承認を前提に世界中に供給すべく拡張に着手している。同社の米国3工場
(Massachusetts, Michigan and Missouri) とベルギーのPuurs工場を製造工場に決め、更に追加工場を決める。2020年に数百万本を供給、2021年に数億本分に増やす。
BioNTechも既存のドイツのMainz及び Idar-Oberstein工場で能力増強を図る。
承認取得後、BioNTech と Pfizer は中国を除く世界全体で共同で販売する。
ーーー
世界で開発中の新型コロナウイルスワクチンは70種類に上るとされる。
米国のModerna, Inc.
がmRNAワクチン「mRNA-1273」の臨床試験(Phase 1) を行っている。
同社は4月16日、開発加速のため米厚生省の生物医学先端研究開発局から最大4億8300万ドルの拠出を受けると発表した。
付記
スイスの製薬会社Lonzaは5月1日、Modernaのワクチン「mRNA-1273」の製造契約を締結したと発表した。
7月にもLonza
U.S. で製造した最初のバッチを供給する。
また、INOVIO Pharmaceuticals
がDNAワクチン「INO-4800」の臨床試験(Phase 1)を行っている。
中国では、Cansino
Biologics(康希諾生物)と中国人民解放軍軍事科学院軍事医学研究院生物工程研究所が共同開発したウイルスベクターワクチンが第2相試験の段階にある。
2020/5/8
主要企業の2020年3月決算
ー 信越化学
2020年3月期は増収増益で、営業損益、経常損益、当期損益とも10年連続増益で、いずれも3期連続の最高益になった。
Shintechが減益となったが、半導体シリコンの増益で補った。
2021年3月期については、コロナ禍がいつどのように終息するか、世界経済への毀損がどのぐらいになるのか、現時点では見通せないため、未定とした。
|
単位:億円 (配当:円) |
| |
売上高 |
営業損益 |
経常損益 |
株主帰属
当期損益 |
配当 |
| 中間 |
期末 |
|
2017/3 |
12,374 |
2,386 |
2,421 |
1,759 |
60 |
60 |
|
2018/3 |
14,414 |
3,368 |
3,403 |
2,662 |
65 |
75 |
|
2019/3 |
15,940 |
4,037 |
4,153 |
3,091 |
100 |
100 |
|
2020/3 |
15,435 |
4,060 |
4,182 |
3,140 |
110 |
110 |
| 前年比 |
-505 |
23 |
29 |
49 |
10 |
10 |
|
2021/3予 |
未定 |
|
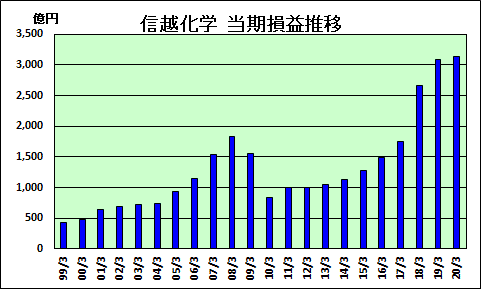
2008年3月期以降の減益については
2019/5/1 主要企業の2019年3月決算ー信越化学 の後半参照
年間配当は5期連続での増配で、2015年3月期までの100円から220円とした。
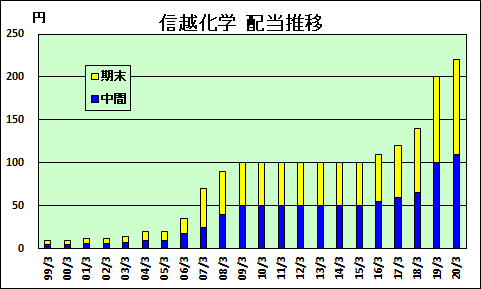
営業損益は下記の通り。
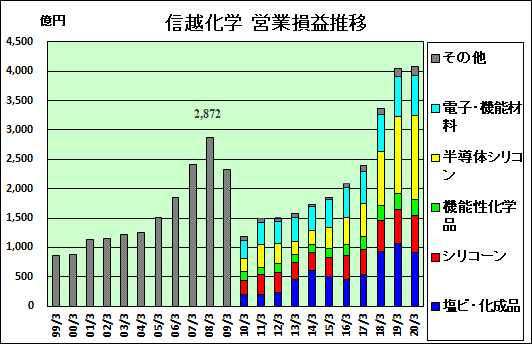
営業損益推移 (単位:億円)
| セグメント |
17/3 |
18/3 |
19/3 |
20/3 |
増減 |
|
|
塩ビ・化成品 |
532 |
932 |
1,065 |
922 |
-143 |
シンテックは高水準の出荷を継続したが、市況の影響を受け減収減益(下記)。 |
|
シリコーン |
425 |
520 |
585 |
615 |
29 |
汎用製品の価格下落 |
|
機能性化学品 |
222 |
257 |
266 |
277 |
11 |
|
|
半導体シリコン |
560 |
930 |
1,320 |
1,433 |
113 |
販売価格と出荷水準の維持 |
|
電子・機能材料 |
552 |
616 |
670 |
685 |
15 |
|
|
その他 |
96 |
115 |
133 |
148 |
15 |
|
|
全社 |
-1 |
-2 |
-3 |
-20 |
-18 |
|
|
合計 |
2,386 |
3,368 |
4,037 |
4,060 |
23 |
|
シンテックのエチレンプラントは商業生産を開始、順調に稼働している。塩ビ樹脂の増設計画は第三期まであり、第一期分の工事が進行中。
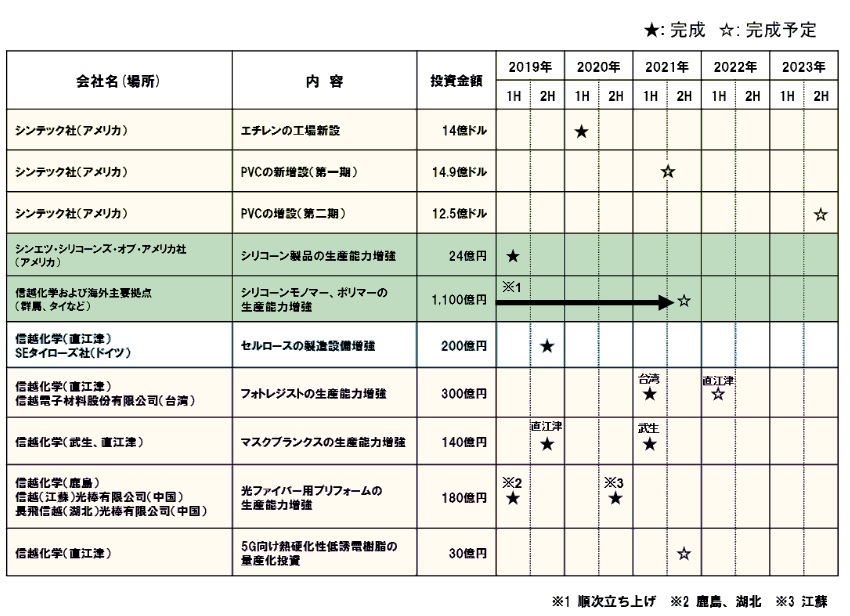
Shintechの損益は下記の通りで、減収減益となった。
(前回、発表なしとしたが、掲載場所が変わっただけで、発表されていた。)
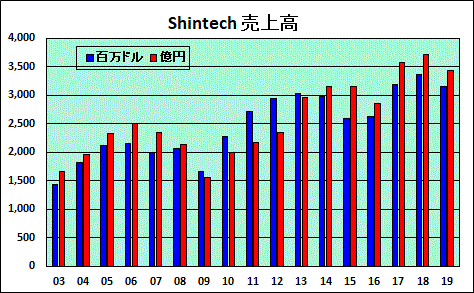
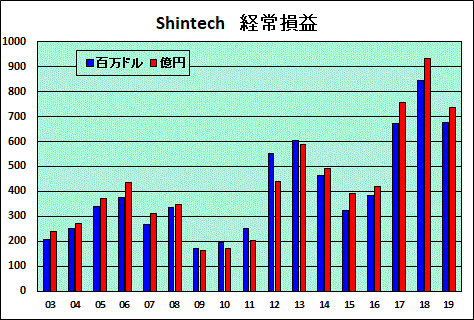
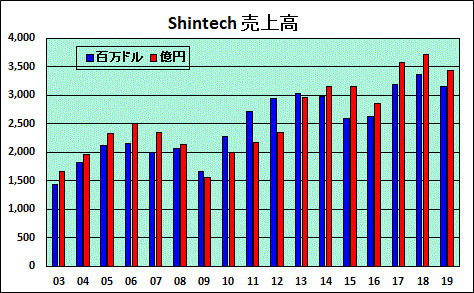
今後は、エチレン新設(2020年上半期稼働)と電解からPVCまでの一貫生産(第一期が2020年末完成)により更なる増益が期待される。
Shintech の能力は次の通りとなる。単位:万トン
| 立地 |
PVC |
VCM |
カ性ソーダ |
エチレン |
| Texas州 |
Freeport |
145 |
- |
- |
|
|
Louisiana州 |
Addis |
58 |
- |
- |
|
|
Plaquemine |
60 |
160 |
106 |
|
| |
2013/6 増設 |
32 |
30 |
20 |
|
|
手直し |
|
|
4 |
|
|
2020初め 完成 |
|
|
|
50 |
|
(認可取得) |
|
(86) |
(66) |
|
|
2020年末 完成 |
29 |
?
|
27 |
|
| 今回増設後合計 |
324 |
? |
157 |
50 |
2020/5/8 インドのLG Chem でスチレンモノマーが漏出、少なくとも11人が死亡
インドのAndhra Pradesh州のVisakhapatnamのLG Polymers Indiaで5月7日の未明
2時半頃に、ガスが漏出し、これによって少なくとも子供を含む11人が死亡して数百人がけがをした。
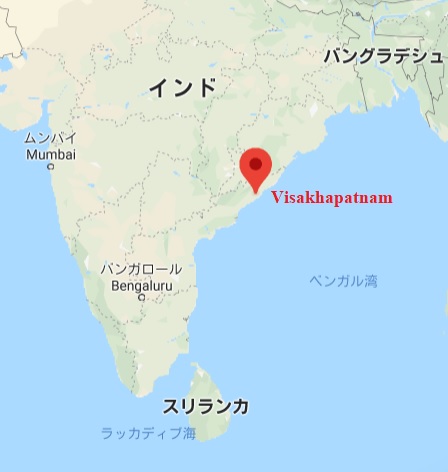

APは「スチレンが工場から流出し、周辺4kmの住民が被害を受けた。これによって一部の住民は路上で倒れ、一部は病院に運ばれた。11人が死亡し、近隣3キロメートル範囲にいた1000人ほどの人々が呼吸困難や目の痛みなどを訴えている」と報じた。死亡者の中には8歳の少女もおり、脱出のために家の2階から飛び降りて亡くなった人もいると伝えた。睡眠中の住民の被害を増やした。
他の報道では「200人から500人が近隣の病院で治療中」で、「このうち70人以上は意識がない状態」としている。
モディ首相はツイッターで「事故現場の状況について、内務省および国家災難管理局の関係者と話を交わした。状況を綿密にモニタリング中」と述べた。
LG Chemは「現在、現地地域住民の被害現況を確認し、住民や役職員の保護のために最大限必要な措置を関係機関と共に取っている」と述べた。
この工場は新型コロナウイルスによるロックダウンで6週間休止しており、操業再開の準備中であった。タンクの周辺には誰もいなかったとされる。従業員の死亡はない。
州政府の役人は、未熟練の労働者がメンテ作業でミスをし、ガスが漏れたと推測している。
2020/5/9 米国で数千人に珍現象「thinkihadititis」
Washington Post は5月7日、数多くの米国人が、自身は以前に新型コロナウイルス感染症にかかっていたと確信する現象が起こっていると報じた。
So many people are convinced that they had covid-19 already
カリフォルニア州の女性は昨年の感謝祭の1週間前に新型コロナと同じ症状に襲われた。2週間自宅で休養すると、症状は急に収まった。
その2カ月後にカリフォルニア州で最初のCOVID-19の患者が出た。
インフルエンザや風邪とCOVID-19の症状に似たところがあるが、
彼女は、みんなが知るまえにCOVID-19が発生しており、自分もそれに罹ったのではと思っている。
同じように考えている人が多数存在するという。
同紙は、COVID-19が問題になる前にこの病気に罹っていたと考える現象を「thinkihadititis」と呼んでいる。
「Think I had it」病(itis )=「私はそれに罹った」病である。多くの人が ‘I think I had it, I think I had it’ と叫んでいるという。
有名人に多いという。
最近の抗体検査で、COVID-19に罹った人よりもはるかに多い人で抗体が見つかっている。
COVID-19には罹りたくないが、すでに新型コロナを体験しているため体内に抗体が生成されている筈だとの希望がこの現象を生ん
でいるという。
(但し、WHOは抗体ができても再度罹らないとの保証はないと警告している。)
ーーー
別記事で、4月30日に新型コロナウイルスの抗体検査で陽性だったことを明かした米歌手のマドンナが、5月2日に自宅待機命令を無視して友人の誕生日パーティーに出席していたことが発覚し、批判を呼んでいる。
2月22日に仏パリで公演を行った後、けがによる不調を理由にその後のツアーを中止。そして感染予防として3月10日と11日に同地で行われる予定だった最終公演も中止したが、実際には自身も含めてツアースタッフの多くが体調不良だったこ
2月22日に仏パリで公演を行った後、その後のツアーを中止したが、実際には自身も含めてツアースタッフの多くが体調不良だったという。
2月22日に仏パリで公演を行った後、けがによる不調を理由にその後のツアーを中止。そして感染予防として3月10日と11日に同地で行われる予定だった最終公演も中止したが、実際には自身も含めてツアースタッフの多くが体調不良だったこ
2月22日に仏パリで公演を行った後、けがによる不調を理由にその後のツアーを中止。そして感染予防として3月10日と11日に同地で行われる予定だった最終公演も中止したが、実際には自身も含めてツアースタッフの多くが体調不良だったこ
マドンナは3月末に「新型コロナは富裕層も賢い人も感染する。平等をもたらすのは素晴らしい」などと投稿し、物議を醸していた。
2020/5/11 住友化学、臭気検知デバイスを用いた新型コロナウイルス感染症の迅速診断センサー開発のため資金提供
住友化学は5月8日、高精度の臭気検知IoTプラットフォームを開発する
イスラエル
のNanoScent社へ、同社が進める臭気検知デバイスを用いた新型コロナウイルス感染症の迅速診断センサー開発のため、必要資金の約7割を提供すると発表した。
NanoScentは、2017年設立のテクニオン・イスラエル工科大学発のスタートアップ企業で、Scent Recognition as a
Serviceというコンセプトのもと、臭気検知のハードウェアのみならずソフトウェア開発も行っている。
NanoScent はケミレジスタ(chemiresistor)を搭載した臭気検知デバイスとデジタル技術を融合したさまざまな新型センサーを開発してい
る。
ケミレジスタとは絶縁性または半導体性の媒体中に導電性材料を混合した材料で,物質の吸着など周辺の化学的環境により導電パスの状態が変化し電気伝導性が変化するため、さまざまな物質を検知するセンサーとして活用できる。一般にナノテクノロジーを活用した材料が用いられる。
複数の臭気をリアルタイムで検知できるポータブルデバイスと、検知したデータをクラウド上に蓄積・解析し、スマートフォンなどの端末にその結果を表示させる情報基盤の試作品を完成させている。同社のNanoScent
SR (Scent Recorder) は直径1mm の8つのセンサーを持つ。
NanoScent は、新型コロナウイルス感染症の拡大抑止に向けて、この技術を活用し、鼻の呼気からウイルス感染を検知できる迅速診断センサーの開発に着手した。
国境や空港、病院などでの感染スクリーニングシステム構築のため、イスラエルおよび欧州の病院や高精度な検査技術を開発する企業と連携し、実証実験を始めている。
臭気検知デバイスを用いた非侵襲(生体を傷つけない)かつ即時に判定ができる極めて簡便な診断方法と、PCR法などのより高精度な検査方法を組み合わせて、「短時間」「低コスト」「高精度」で実施可能な感染スクリーニングシステムの実現を目指
す。
住友化学は、迅速診断センサー技術の開発は、新型コロナウイルス感染症はもとより、将来に発生が懸念されるパンデミック対策にも応用が可能であると考えている。
ーーー
住友化学は2019年12月にNanoScent に200万ドルを出資し、戦略的な技術的連携を深めるとともに、新規ヘルスケア事業の創出に取り組むこととした。
住友化学は連携により、次世代ヘルスケアプラットフォームの鍵となる「体調可視化」の実現を目指している。
排泄物の臭気データから体調変化や病気の兆候を読み取り、その日の体調に適したソリューション(食事や薬、生活習慣など)の提案により、健康管理に役立てる仕組みを構築すべく、実証実験を計画している。
また、さまざまな揮発性化学物質の集合体である臭気を高精度で検知できるNanoScent
の技術は、ヘルスケアに留まらず、工場や街中での有害物質の検知・モニタリング、自動車内の臭気判定・管理など、応用範囲は多岐にわたるため、次世代事業の創出につながると判断した。
ーーー
臭いによる新型コロナウイルスの感知は全く新しい方法である。
現在、新型コロナウイルスの検査には、PCR検査、抗原検査、抗体検査がある。
PCR検査と抗原検査は、人体に侵入したウイルスを検査し、抗体検査は、人間が持つウイルスへの抗体を検査する。
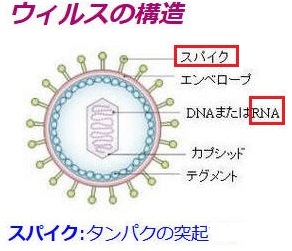
PCR検査はウイルスのRNAの存在を検査する。ウイルスは、デオキシリボ核酸(DNA)を持つDNAウイルスと、リボ核酸 (RNA)をゲノムとするRNAウイルスに分けられる。
コロナウイルスはRNAウイルスなので、PCR法の前にRNAをDNAに変える「逆転写」という作業を行う。
次に、一本のDNAをもとに、次々にDNAを複製する。
PCR法では、検体に含まれるウイルスの遺伝子量では検出できないが、増幅することにより検出できるようになる。
2020/2/29
COVID-19 ウイルス、迅速検出
抗原検査は、ウイルスの外側に付いている突起部分(スパイク)のたんぱく質を検出する。抗原は、免疫細胞上の抗原レセプターに結合し、免疫反応を引き起こさせる物質の総称。
米食品医薬品局(FDA)は5月9日、新型コロナウイルスに感染しているか簡易診断できる「抗原検査」に初めて緊急使用認可を与えたと発表した。
米Quidel
Corporationが手掛ける抗原検査Sofia®
2 SARS Antigen FIAで、同社のSofia
2 Fluorescent Immunoassay Analyzer で検査する。
抗原検査は鼻の奥から綿棒で粘液を採取し、ウイルス特有のたんぱく質を検出する。
「PCR検査」より精度は劣るものの、検査現場で15分で判定できるほか、コストが安いのも利点である。
厚労省は富士レビオの抗原検査キットを5月13日に薬事承認し、保険適用する。15~30分で検出する。精度はやや劣るため、陰性が出た場合は、念のためPCRによる検査を実施する見通し。
ヒトがウイルスに感染すると、まずlgM抗体ができ、短期間で消失する。lgM抗体に遅れてlgG抗体ができ、漸減しながら長期間持続する。
抗体検査は、この抗体を検査する。
2020/5/7 米FDA、ロシュの新型コロナ抗体検査薬の緊急使用許可
2020/5/12
東京大学、アビガンとフサンの併用療法の臨床研究開始
東京大学医学部附属病院は5月8日、肺炎を発症している新型コロナウイルス(SARS-CoV-2)陽性患者を対象に、ファビピラビル(アビガン®錠200mg)とナファモスタットメシル酸塩(注射用フサン®50)の併用療法の特定臨床研究を開始したと発表した。
付記
東大医学部附属病院は7月6日、重症患者へのナファモスタットメシル酸塩(商品名フサン他)、ファビピラビル(商品名アビガン)併用療法の観察研究の結果を発表した。
患者11例中10例で症状の軽快が見られ「併用の有効性を示唆する」としている。結果は3日付の医学誌『クリティカル・ケア』(電子版)に掲載された。
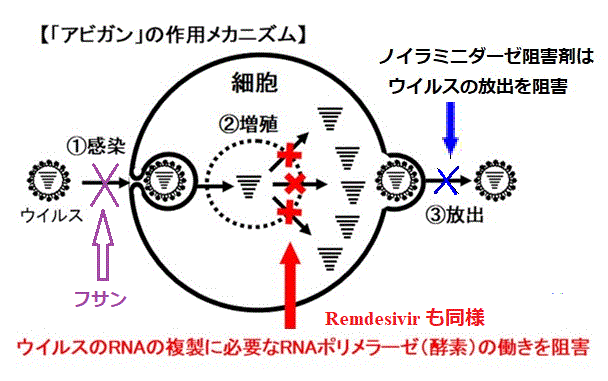
現在、治療に用いられている抗ウイルス剤はノイラミニダーゼ阻害剤(Neuraminidase
inhibitors)で、増殖されたウイルスの放出を阻害して感染の拡大を防ぐものだが、アビガンは、ウイルスの細胞内での遺伝子複製を阻害することで増殖を防ぐRNAポリメラーゼ阻害剤である。Remdesivir
も同じくRNAポリメラーゼ阻害剤である。
ある報告では、投与開始14日後に重症患者の6割が改善、軽症や中等症では9割の患者で改善が認められた。
2020/4/21
アビガン投与で重症患者6割、軽中等症患者9割が改善
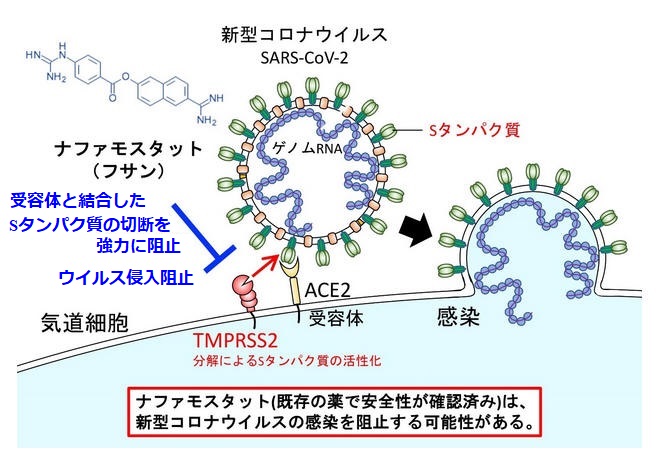
東京大・医科学研究所の井上純一郎教授らは3月18日、急性膵炎の治療薬として国内で長年使われてきた点滴薬剤「ナファモスタット(商品名フサン)」が新型コロナウイルスの感染を阻止する可能性があると発表した。
ウイルスが人体に感染するには細胞の表面に存在する受容体タンパク質(ACE2受容体)に結合したのち、ウイルス外膜と細胞膜の融合を起こすことが重要である。
コロナウイルスの場合、ウイルスのSタンパク質がヒト細胞の細胞膜のACE2受容体に結合したあとに、タンパク質分解酵素(TMPRSS2)で切断され、Sタンパク質が活性化されることが重要であるが、ナファモスタット(フサン)はTMPRSS2による切断を阻止し、ウイルスの侵入を阻止する。
2020/3/18
急性膵炎治療薬が新型コロナウイルス感染阻止の可能性
フサン(感染阻止)とアビガン(増殖阻止)は、作用部位が異なるため、両者を併用することで相加的な効果が得られることが期待される。
また、新型コロナウイルス感染症の一部の患者では血管内での病的な血液凝固が病気の悪化に関与していると考えられ、フサンの抗凝固作用が有効であると期待できる。
本試験は東京大学医学部附属病院のほか、多施設共同で実施する。
対象は肺炎を有するCOVID-19患者で、20~74歳の男女。
アビガンとフサンの併用群と、アビガン単独群の二群で薬剤の作用を比較し、想定される有効性や安全性が認められるか確認する。
付記
鳥居製薬からフサンを承継した日医工は5月18日、フサンの増産を発表した。
現在は鳥居製薬(日本たばこ産業子会社)に委託し、年65万本程度生産しているが、能力の100万本まで増産する。
別途、自社の愛知工場に40億円をかけて年内に稼働、委託分を含め能力を年300万本にする。
2020/5/13
サウジアラビア、緊縮策を実施&追加の自主減産
サウジアラビアは、原油価格の急落や新型コロナウイルス感染拡大による経済への影響で打撃を受けている国家財政を強化する取り組みの一環として、生活費手当の停止や付加価値税(VAT)引き上げを実施する。国営通信が11日、政府の声明を伝えた。
生活費手当は6月1日に停止され、VATは7月1日に現在の5%から15%に引き上げられる。
サウジアラビアは、原油価格の急落や新型コロナウイルス感染拡大による経済への影響で打撃を受けている国家財政を強化する取り組みの一環として、生活費手当の停止や付加価値税(VAT)引き上げを実施する。国営通信が11日、政府の声明を伝えた。
生活費手当は6月1日に停止され、VATは7月1日に現在の5%から15%に引き上げられる。
サウジアラビアは、原油価格の急落や新型コロナウイルス感染拡大による経済への影響で打撃を受けている国家財政を強化する取り組みの一環として、生活費手当の停止や付加価値税(VAT)引き上げを実施する。国営通信が11日、政府の声明を伝えた。
生活費手当は6月1日に停止され、VATは7月1日に現在の5%から15%に引き上げられる。
サウジアラビア政府は、原油価格急落と新型コロナウイルスの感染拡大が財政に及ぼす影響とに対応するため、一連の緊縮措置を発表した。
サウジ財務省は5月11日、声明を発表し、世界的な需要の落ち込みによって原油価格が低迷し、国の歳入が大幅に減少している一方、新型コロナウイルスの感染拡大が続き、医療費などの負担が増えているとし、財政の安定化に向けた新たな措置をとると明らかにした。
サウジの財政均衡に必要な原油価格は1バレル=80ドル超程度とされる。
第1四半期で石油収入は24%減の343億ドルとなり、支出が収入を超過し、90.9億ドルの赤字となった。
2019年第Ⅰ四半期は74億ドルの黒字であった。.
1) 付加価値税引き上げ
Saudi Arabia は2018年1月1日から付加価値税(VAT)を導入した。
税率は5%で、食品を含むほとんどの財とサービスに適用される。
2018/1/4
サウジとUAE、1月から付加価値税導入
今回、7月1日からこれを一気に3倍の15%へ引き上げる。
2) 政府職員の生活費手当の撤廃
2018年のVAT導入に際し、物価上昇の影響を緩和するため、政府職員に1カ月1000リヤル($267)の生活費手当を支給した。
今回、これを6月1日に廃止する。
3) その他 公共事業の中止、延期など
ムハンマド皇太子の「ビジョン2030」構想の一部プログラムの予算も縮小する。
歳入拡大・歳出削減措置の規模は合わせておよそ1000億リヤル(約2兆8500億円)となる。
ジャドアーン財務相は、「本日の措置は痛みをもたらすかもしれないが、財政と経済の短・長期的安定性を守るために必要であり、助けになる」と説明した。
ーーー
サウジアラビアは5月11日、自発的かつ一方的に日量100万バレルの減産を実施すると発表した。
OPECプラスは4月12日、5月と6月について日量970万バレルの減産で最終合意した。7~12月は770万バレル、2021/1~2022/4月は580万バレルにする。
サウジとロシアは1,100万バレルを基準とし、250万バレル減らし、850万バレルとする。
2020/4/13
OPECプラス協調減産、日量970万バレルで最終合意
今回、サウジは6月の生産量目標を日量750万バレル弱とする。ブルームバーグのデータによると、これは2002年半ば以来の低水準となる。
サウジのエネルギー省当局者は「今回の追加減産を通じ、サウジは世界の石油市場の安定に取り組み、OPECプラスの参加国やその他の産油国にこれまでの約束を守るとともに自発的な追加減産実施を促すことを目指す」と説明した。
2020/5/14
Tesla、地方政府の規則に反して生産を再開
米TeslaのElon Musk CEOは5月11日、カリフォルニア州Alameda
CountyのFremont
市のEV工場が同日から生産を再開すると明らかにした。
カリフォルニア州のNewsom
知事は3月19日、新型コロナウイルスの感染対策として、約4000万人の全住民に対し、食料の買い出しや通院など必要な場合を除き自宅にとどまるよう命じた。感染が住民の半数以上に広がる恐れがあるとして、医療体制の崩壊を防ぐため、期限を定めずに大規模な外出禁止に踏み切った。
アラメダ郡を含む周辺自治体は3月中旬から外出制限を始めた。Teslaは外出制限後もEV工場の操業を続けていたが、同郡が「Teslaは命令で定めた必要不可欠な業種ではない」との判断を示したことで3月下旬から操業停止を余儀なくされていた。CEOは外出禁止令について「ファシストだ」と強い不満を示していた。
カリフォルニア州は8日、新型コロナウイルス対策で3月19日に発令した外出禁止令を50日ぶりに緩和し、一部の店舗について営業再開を許可した
カリフォルニア州は8日、新型コロナウイルス対策で3月19日に発令した外出禁止令を50日ぶりに緩和し、一部の店舗について営業再開を許可した
カリフォルニア州は5月8日、新型コロナウイルス対策で3月19日に発令した外出禁止令を50日ぶりに緩和し、書店や衣料品店、生花店など一部の店舗について営業再開を許可した。
自動車産業が集積する米ミシガン州はすでに自動車関連工場の再開を認めており、GMなどの自動車大手は5月18日から段階的に生産を再開する計画を表明している。
カリフォルニア州のNewsom知事も5月8日、一部工場の操業再開を認めると表明した。
Tesla は5月9日、操業再開プロセスに着手したと明らかにした。
しかし、これに対しアラメダ郡は6月1日までテスラの工場再開を認めないことを伝えた。
州政府は市や郡などの自治体がより厳しい独自ルールを設けることを認めている。シリコンバレー周辺の自治体は、医療機関向けの防護服が不足しているなどとして5月8日以降も行動制限を続けると表明した。
TeslaのMusk CEOは5月9日、アラメダ郡が工場再開を認めないことへの対応として、ツイッター
で「Teslaは郡に対し直ちに訴訟を起こす。選出されたわけでもない無知な暫定保健担当官は州知事や米大統領、憲法の自由、そして常識に反する行動をとっている」と述べた。
Teslaは同日、工場の再開を認めなかったことを巡り、
郡の外出禁止令は行き過ぎで憲法で保障された法の下の平等にも反するなどとし、命令の停止などを求め、サンフランシスコ連邦地裁に訴訟を提起した。f
またCEOは「我慢の限界だ」と述べ、カリフォルニア州パロアルト市にあるTesla本社について「テキサス州かネバダ州に即座に移転する」ともツイートした。(パロアルト市長はTeslaへの支援を表明した。)
フリーモント工場を残すかどうかも、「将来的にTeslaがどういう扱いを受けるかによる」と移転をちらつかせた。
メディアによると、フリーモント市のTeslaのEV工場では5月11日朝から従業員らが出勤を始めていた。CEOは「誰かが逮捕されるとしたら、私だけであることを願う」とも書き込んだ。
Tesla is restarting production today against Alameda County rules.
I will be on the line with everyone else.
If anyone is arrested, I ask that it only be me.
トランプ大統領は5月12日、ツイッターに「テスラの工場を再開させるべきだ。安全にすばやく再開させることができる」と投稿し、地元自治体に対して早期に再開を認めるよう促した。
California should let Tesla & Elon Musk open the plant, NOW.
It can be done Fast & Safely!
付記
アラメダ郡の公衆衛生当局は5月12日、フリーモント工場の再開に関して、Tesla と合意に達した、と発表した。Tesla
が提出した感染拡大防止策を精査し、安全面でいくつかの追加の対策を施すことなどを条件に、工場再開で合意した。フリーモント工場の生産再開は、5月18日からとなる予定。
フリーモント工場は、もともとトヨタ自動車とGMの合弁会社「NUMMI」の工場であった。GMの経営破綻を機に合弁は解消され、2010年4月に操業を停止。その後、Teslaの工場になった。
同社にとって米国で唯一の完成車の組み立て拠点で、年産能力は約49万台。従業員は1万人を超える。

目次 次へ























